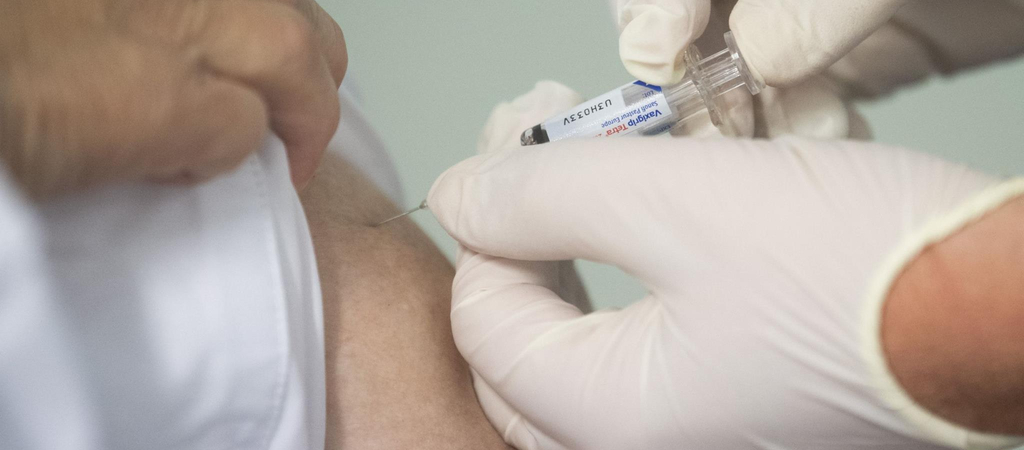
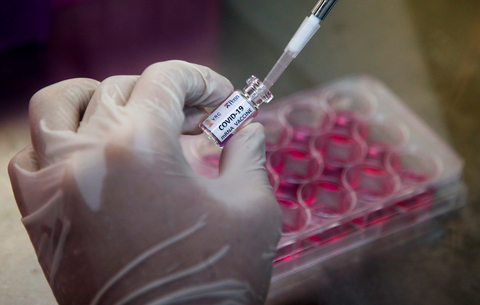
Beadta a kérelmet az amerikai gyógyszerügyi hivatalhoz a BioNtech és a Pfizer a koronavírus elleni vakcinájuk sürgősségi engedélyeztetésére.
Beadta a kérelmet vakcinájuk engedélyeztetésére a BioNtech és a Pfizer gyógyszergyártó csoport az Egyesült Államok Élelmiszer- és Gyógyszerügyi Hivatalához (FDA) – írja a CNN. A vakcinagyártók sürgősségi engedélyért folyamodnak, hogy a vakcina minél hamarabb elérhetővé váljon.
A cégcsoport szerint vakcinájuk, a BNT162b2 már idén decemberben elérhető lehet a koronavírus miatt veszélyeztetett csoportba tartozó emberek számára. Hatása ugyanakkor így is csak jövőre lehet a járvány terjedésére: ahhoz, hogy immunizáljon valakit a koronavírusra, két oltásra van szükség, egymástól néhány hét távolságra. A védelem az első oltást követően 28 nappal érhető el.
A BioNtech és a Pfizer e hónap elején jelentette be, hogy közösen kifejlesztett oltóanyaguk hatékonysága az eddigi klinikai próbák és vizsgálatok eredményei alapján eléri a 94 százalékot azoknál az idősebb felnőtteknél is, akikre különösen veszélyesek a vírus okozta betegség szövődményei.
Nemrég azt is közölték, hogy napokon belül folyamodnak majd az FDA engedélyéért. A New York Times akkor azt írta, ha az FDA engedélyezi az oltóanyagot, akkor idén akár 50 millió, a jövő év végéig pedig 1,3 milliárd adag vakcina is elkészülhet.
Az Egyesült Államokban ez az első koronavírus elleni oltás, amelyik már az engedélyeztetés szakaszába ért.

 Ajándékozz éves hvg360 előfizetést!
Ajándékozz éves hvg360 előfizetést!